В последние десятилетия установлено, что в патогенезе рожи, как и других инфекционных заболеваний, важная роль принадлежит нарушениям иммунного гомеостаза, в том числе и генетически обусловленным [7,8]. В настоящее время большое внимание уделяется изучению роли цитокинов в патогенезе и клинических проявлений заболеваний, которая во многом зависит от существования аллелей генов цитокинов и рецепторов к ним. Доказана взаимосвязь аллельных вариантов генов цитокинов с тяжестью и продолжительностью заболеваний, их исходами [11,14,15, 18].
Установлено, что структурные особенности белковых продуктов полиморфных генов цитокинов ведут к различному качеству иммунного ответа организма на различные воздействия [12,19]. Известно, что уровень продукции некоторых цитокинов ассоциирован с определёнными аллелями этих цитокинов. Например, аллель А в G308А гена фактора некроза опухолей – α (ФНО-а) и аллель Т С589Т интерлейкина–4 (ИЛ-4) ответственны за повышенную транскрипцию генов, в результате чего повышается продукция цитокина ФНО-а и ИЛ–4. Значительное повышение концентрации данных цитокинов способствует быстрому прогрессированию заболевания и более тяжёлому течению. Для гена интерлейкина-10 (ИЛ-10) определяется замена в трёх участках: -1082, -819,-592 [11,13]. При этом аллель А в С592А и G1082А гена интерлейкина-10 способствует сниженной продукции ИЛ-10, который являясь провоспалительным цитокином, оказывает блокирующее действие на клетки Th-1 типа, снижая, таким образом, синтез провоспалительных цитокинов. В случае низкого уровня интерлейкина-10 поддерживается высокая концентрация провоспалительных цитокинов, что также проводит к неблагоприятному течению заболевания. Интерлейкин-10 индуцирует пролиферацию тимоцитов в присутствии интерлейкина-2 и интерлейкина-4. Огромную роль во взаимодействии клеточных и гуморальных факторов иммунных и воспалительных реакций играет интерлейкин – 4 [6]. Для гена интерлейкина - 4 обнаружен полиморфизм в интронах 2 и 3, в промоторном участке позиции - 590 (замена С на Т). Для полиморфизма С590Т интерлейкина-4 выявлено преобладание гетерозиготного С/Т варианта.
Важную роль в реализации механизмов иммунного ответа играет интерлейкин-2 , продуцентами которого являются Th1-клетки. Следовательно, развитие и течение рожи может зависеть от полиморфизма генов, в том числе – интерлейкина-2.
Целью исследования стало изучение встречаемости полиморфизма промотора гена интерлейкина-2 (Т330G) и оценка его клинико-прогности-ческого значения для прогрессирования инфекционного процесса при роже.
Материалы и методы. Нами были обследованы 90 русских пациентов с рожей, проживающих на территории Забайкальского края. В работе с обследуемыми лицами соблюдались этические принципы, предъявляемые Хельсинкской Декларацией Всемирной Медицинской Ассоциации (World Medical Association Declaration of Helsinki и Правилами клинической практики в Российской Федерации, утвержденными Приказом Минздравсоцразвития РФ от 19.06.2003 г.№ 266.
Диагноз установлен на основании клинико-анамнестических данных согласно классификации В.Л. Черкасова (1986) [17]. Клиническое проявление заболевания было типичным и характеризовалось лихорадкой, ознобами и другими симптомами интоксикации, появлением на коже яркой гиперемии и отёка, болезненности поражённого участка при пальпации, регионарного лимфаденита.
Критерии исключения – наличие тяжёлой соматической патологии, осложнённое, повторное или рецидивирующее течение, распространенность процесса. Пациенты распределялись по характеру локальных изменений на 2 группы: основную (50 пациентов с первичной рожей эритематозной формой заболевания) и сравнения (50 больных – с первичной рожей буллёзно-геморрагической формой). В качестве контрольной группы обследовано 100 условно-здоровых жителей Забайкалья. Группы сопоставимы по половым и возрастным характеристикам.
Определение полиморфизма промотора гена интерлейкуина -2 (Т330G) осуществлялось методом полимеразной цепной реакции (ПЦР) с использованием праймеров ООО «Литех» (г. Москва). Анализу подвергалась геномная ДНК, выделенная из лейкоцитов цельной крови с помощью реагента «ДНК-экспресс-кровь», затем проводилась реакция амплификации с двумя парами аллель-специфических праймеров. Анализ продуктов амплификации произведен методом электрофореза. Для проведения электрофореза использовался 3% агарозный гель, визуализация с помощью 1% бромистого этидия в ультрафиолетовом свете.
Полученные данные обработаны с помощью пакетов программ BIOSTAT, STATISTICA 6,0 (StatSoft Inc., США), с определением достоверности различий при достигнутом уровне значимости p<0,05. Для сравнения частот применялись: критерий χ2 (Пирсона). Для определения частот аллельных вариантов генов применялся закон Харди-Вайнберга [10].
Результаты и обсуждение. В результате проведенного анализа полиморфизма промотора гена интерлейкина-2 (Т330G) у больных с эритематозной и буллёзно-геморрагической формами первичной рожи и у здоровых лиц установлено следующее (табл. 1.).
Встречаемость генотипа Т/G преобладает в контрольной группе, тогда как у заболевших рожей превалирует нормозиготный вариант (Т/Т). При этом в группе больных с эртематозной формой рожи частота Т/Т варианта выше почти в 1,5 раза, чем в группе больных с буллёзно-геморрагической и в 20 раз (53% и 3%) по сравнению с группой контроля.
С целью выявления ассоциации полиморфного маркера промотора интерлейкина-2 в участке Т330G с заболеванием рожей изучено распределение аллелей и генотипов (табл. 2).
Таблица 1. Частота встречаемости полиморфных маркёров Т330G в гене интерлейкина-2 у больных рожей в Забайкальском крае
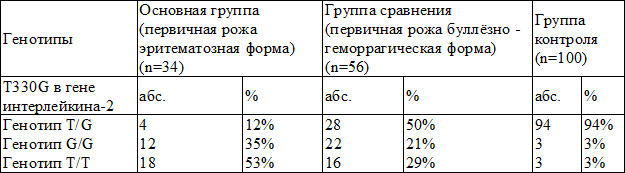
Таблица 2. Относительные и абсолютные частоты генотипов интерлейкина-2 (Т330G)
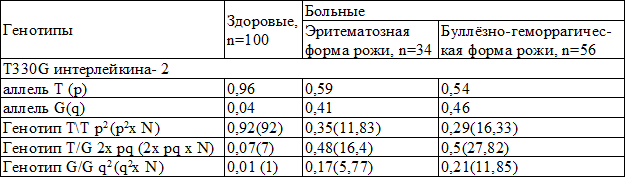
Примечания: p2, 2х pq, q2 – относительная частота генотипа; p2х N, 2х pq х N, q2х N – абсолютная частота генотипа (N – общее число наблюдений)
Обнаружено, что у больных рожей аллели G и Т полиморфизма Т330G промоторного участка гена интерлейкина-2 встречаются практически с одинаковой частотой. При этом по сравнению с контрольной группой у больных преобладал гетерозиготный вариант T/G, особенно при буллёзно-геморраги-ческой форме заболевания (0,5). В группе контроля чаще выявлялся генотип Т/Т (0,92). Известно, что различные полиморфные варианты генов цитокинов могут сказываться на их продукции медиаторов иммунного ответа.
Это в свою очередь влияет на направленность иммунного ответа, своевременность и эффективность межклеточной сигнализации [5,6]. Полиморфизм генов цитокинов является существенным фактором предрасположенности (резистентности) к инфицированию, развитию заболевания и длительному течению с осложнениями. Большую роль в этом играют не только отдельные аллели генов, но и их сочетание. Например, аллель А в G308А гена ФНО-α и аллель Т и С589Т интерлейкина –4 ответственны за повышенную транскрипцию, в результате чего повышается продукция ФНО-α и интерлейкина-4. Значительное повышение концентрации данных цитокинов способствует быстрому прогрессированию гепатита С и более тяжёлому его течению. При этом аллель А в С592A и G1082А гена интерлейкина-10 способствует сниженной продукции данного интерлейкина. Ранее показано, что наличие аллели А в С592A и G1082А гена интерлейкина-10 у больных коклюшем способствуют сниженной продукции IL-10 и развитию осложнений заболевания [9]. У детей с Т/Т вариантом участка С589Т гена интерлейкина-4 продукция IL-4 IgМ и IgA более высокая, в сравнении с носителями нормальных гомозигот и гетерозигот. Для обладателей полиморфных маркеров в участке G1082A интерлейкина-10, в случае неосложненного течения, также характерна гиперпродукция противовоспалительных цитокинов. Носители А/А варианта С592А гена интерлейкина-10 отличаются гипопродукцией IL10, IL4, IgM. Наличие полиморфных маркеров в участке G1082A гена интерлейкина-10 ассоциировано со сниженным образованием лимфоцитарно-тромбоцитарных коагрегатов, а, следовательно, и с миграцией иммунокомпетентных клеток в очаг повреждения [1,9].
Ранее мы проследили продукцию различных цитокинов и лимфоцитарно-тромбоцитарную адгезию у больных рожей и оценили их прогностическое значение на течение заболевания [7,8]. Известно, что интерлейкин-2 является главным индуктором лимфоцитпрно-тромбоцитарного взаимодействия [2, 3, 4, 16]. Способность лимфоцитов контактировать с кровяными пластинками отражает степень активации клеточных механизмов иммунологической защиты. Полиморфизм промоторного участка гена интерлейкина-2 сказывается на продукции иммунного цитокина и его концентрации, что в свою очередь влияет на местные клеточные механизмы защиты. Характер их протекания обуславливает генетическую предрасположенность к развитию рожи и склонности к тяжелому течению заболевания.
Таким образом, проведенное исследование полиморфизма промотора гена интерлейкина-2 при роже подтверждает наличие генетических механизмов, касающихся обмена цитокинов. Предполагается, что полиморфные варианты генов интерлейкина-2 (Т330G) повышают риск развития более тяжёлых форм рожи.
Выводы
1. У больных рожей аллель G гена интерлейкина-2 (Т330G) встречается в 10 раз чаще, чем среди здоровых лиц и ее присутствие может предрасполагать к развитию более выраженного местного воспалительного процесса.
2. Распределение генотипов среди больных рожей характеризуется увеличением доли вариантов Т/G и G/G гена интерлейкина-2 (Т330G).
