Актуальность вопроса. Ишемическая болезнь сердца (ИБС) является одной из ведущих проблем здоровья общества и остается основной причиной смертности и инвалидизации населения [1, 2].
Одним из серьезных осложнений ИБС является образование постинфарктной аневризмы левого желудочка (ПАЛЖ), которая формируется у 20–50% больных, перенесших острый инфаркт миокарда [1, 4]. Пятилетняя выживаемость составляет 30-50% [1, 2, 4]. При этом выраженное снижение глобальной сократительной способности левого желудочка (ЛЖ), ниже или равной 30%, сопровождается ещё более низкой 5-летней выживаемостью, 10-15% [1, 4, 6, 7].
В особенно тяжелой степени течения ИБС к ПАЛЖ присоединяется недостаточность митрального клапана (МК), которая наблюдается у 40-50% больных, перенесших острый инфаркт миокарда. При этом, недостаточность МК является независимым предиктором смерти [2, 4, 7] и смертность этих больных коррелирует со степенью дисфункции МК.
Утрата части функционирующего миокарда, сопровождается структурными изменениями, затрагивающие как поврежденные, так и неповрежденные участки миокарда, именуемая как "ремоделирование сердца". Проявлением ремоделирования сердца является: 1) дилатация полости ЛЖ; 2) истончение стенки поврежденной инфарктом; 3) гипертрофия неповрежденного миокарда с увеличением массы миокарда ЛЖ; 4) изменение конфигурации и геометрии ЛЖ.
Присоединение митрального порока, значительно изменяет патофизиологию кровообращения при ИБС, еще в большей степени снижая производительность левого желудочка и ухудшая прогноз заболевания.
Основным компенсаторным механизмом при ПАЛЖ и митральной регургитации является увеличение конечно-диастолического объема (КДО) ЛЖ с одновременным приростом глобальной фракции выброса, что позволяет обеспечить приемлемый баланс антеградного и ретроградного ударного объема.
Изменение геометрии ЛЖ усугубляет митральную регургитацию, за счет смещения оснований папиллярных мышц и растяжения фиброзного кольца.
Для обеспечения достаточного выброса помимо увеличения объема желудочка происходит ремоделирование его полости. Она приобретает более округлую форму (соотношение большой и малой оси становится менее 1,50, в то время как при обычных условиях оно превышает 1,9).
Нарушение функциональных и трехмерных анатомических соотношений структур МК, неблагоприятное распределение зон гипокинезии миокарда становятся основной причиной регургитации [1, 4, 6, 7]. Так как регургитация развивается в течение некоторого времени, имеется возможность развития компенсаторных механизмов.
Объемная перегрузка в условиях скомпрометированного миокарда ведет к дилатации полости и уже затем к дилатации фиброзного кольца [4, 6, 7]. Его расширение может неблагоприятно сказываться на величине регургитации, то есть реализуется принцип «регургитация ведет к регургитации». Все эти механизмы присутствуют у больных с ПАЛЖ в сочетании с митральной регургитации.
При любом варианте митральная недостаточность ведет к объемной перегрузке ЛЖ. Даже при минимальном сбросе этот факт ухудшает прогноз заболевания. Недостаточность МК и ИБС являются взаимоотягощающими патологическими состояниями. Механизм Франка-Старлинга не может быть адекватно реализован в условиях ограниченного коронарного кровотока.
Увеличение размеров фиброзного кольца при ишемической митральной недостаточности носит вторичный характер, обусловленной объемной перегрузкой миокарда. Изолированная дилатация кольца является потенцирующим фактором при нарушениях других клапанных структур, но с течением времени приобретает большее значение, становясь основной причиной ишемической недостаточности МК.
Результаты исследований позволяют утверждать, что для развития митральной недостаточности требуется наличие смещения основания папиллярных мышц, что ведет к ограничению подвижности створок МК в сочетании с дилатацией фиброзного кольца, которое с течением времени приобретает большее значение. Все эти проявления являются следствием изменения геометрии ЛЖ, сопровождающее как ПАЛЖ, так и митральную регургитацию.
Цель исследования. Анализ функции митрального клапан после операции геометрическая реконструкция ЛЖ, реваскуляризация миокарда и коррекции митральной недостаточности.
Клинический материал и методы исследования. Были подвергнуты анализу данные исследования 73 пациента с постинфарктной аневризмой левого желудочка (ПАЛЖ), c сопутствующей митральной недостаточностью той или иной степени, от 2 до 3,5 ст., обследованных и оперированных в Научном центре сердечно-сосудистой хирургии им. А.Н. Бакулева РАМН в период с 1998 по 2010 г.
В группе обследованных больных было 64 (88%) мужчин в возрасте от 49 до 68 лет и 9 (12%) женщин в возрасте от 44 до 58 лет. Средний возраст больных составил в среднем 56±12 лет. Диагноз ПАЛЖ в сочетании с ишемической митральной регургитацией был установлен на основании клинической картины заболевания, анамнеза и данных клинико-инструментальных методов исследования.
Всем больным проводилось общеклиническое обследование, электрокардиография с прекардиальным картированием, суточное Холтеровское мониторирование электрокардиография (ЭКГ), эхокардиография (Эхо КГ), стресс-эхокардиография, коронарография и вентрикулография.
Всем пациентам была выполнена операция - реваскуляризация миокарда с реконструкцией ЛЖ по методике Бокерия-Дора и устранение митральной регургитации в условиях искусственного кровообращения и фармакохолодовой кардиоплегии раствором «кустодиол». Реконструкция митрального клапана (МК) проводилась трансвентрикулярным доступом. В зависимости от механизма возникновения регургитации на митральном клапане, использовались несколько способов пластики - редукция межпапиллярного пространства, аннулопластика по методу Алфиери, а так же имплантация опорного кольца Карпантье в митральную позицию.
Результаты исследования. Положительный клинический эффект операции отмечен у большинства оперированных больных. Сравнительные до и послеоперационные данные сердечной недостаточности по NYHA представлены в табл. 1. Класс сердечной недостаточности снизился с 2,66 до 1,64.
Таблица 1. Сердечная недостаточность по NYHA до и после операции по группам
![]()
Распределение больных по функциональному классу стенокардии до и после операции представлено в табл. 2. Класс стенокардии снизился с 2,5 до 1,7.
Таблица 2. Распределение больных по классу стенокардии до и после операции
![]()
На момент выписки больным проводилось ЭхоКГ исследование для оценки степени митральной недостаточности и сократимости миокарда после операции.
После хирургического лечения отмечено возрастание как общей, так и локальной сократимости. При сравнении до и после операционных данных отмечается прирост общей фракции выброса (ОФВ) с 40,5 до 44,3, уменьшение объемов ЛЖ - конечно-диастолический объем (КДО) с 198,3 до 159,4, конечно-систолический объем (КСО) с 120,9 до 92,7.
Данные ЭхоКГ до и после операции представлены в табл. 3. По сравнению с дооперационными значениями размеры левого предсердия (ЛП), а так же ЛЖ уменьшились. Митральная недостаточность (МН) уменьшилась с 2,6 до 1,5. Диаметр фиброзного кольца митрального клапана (ФК МК) по сравнению с исходными значениями уменьшился с 35,9 до 29,2. Расчетное систолическое давление в легочной артерии (ЛА) так же снизилось.
Таблица 3. Результаты ЭхоКГ после выполненных операций
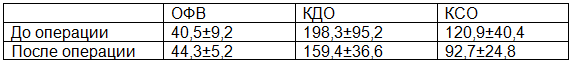
Динамика основных объемных показателей ЛЖ после операции представлены в нижеприведенной табл. 4. После операции была выявлена динамика в основных линейных показателях, характеризующих геометрию ЛЖ у пациентов. Размер длинной оси ЛЖ уменьшился и составил в среднем 8,7±0,2 см (исходно 9,8±0,1).
Таблица 4. Динамика степени митральной недостаточности после операции
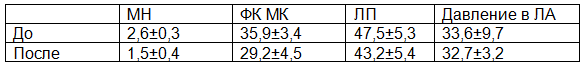
Значительно в меньшей степени отмечалось уменьшение размеров коротких осей ЛЖ. Так, короткая ось на уровне митрального клапана составила 4,6±0,2 см (по сравнению с 5,2±0,1), на уровне папиллярных мышц 5,6±1,0 см (исходно 6,2±0,5), на верхушечном уровне 3,5±0,6 (исходно 4,3±0,6 см).
Соответственно, индекс сферичности на базальном уровне уменьшился и составил 0,52 по сравнению с 0,54 исходно, на среднем уровне - 0,64 при исходном 0,65, на верхушечном уровне - 0,40 при исходном 0,44.
Динамика основных линейных показателей ЛЖ после операции представлены в табл. 5.
Таблица 5. Динамика линейных показателей ЛЖ после операции
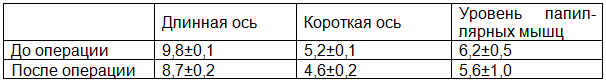
Обсуждение. Пациенты с ПАЛЖ и сопутствующим поражением митрального клапана относятся к тяжелой категории больных и характеризуются тяжелым проявлением коронарной и сердечной недостаточности. Основными механизмами, участвующими в развитии митральной недостаточности является изменение геометрии левого желудочка, вследствие ишемического ремоделирования и нарушения функции сосочковых мышц [1, 2, 5-7].
Хирургические методы пластики МК позволяют выполнить эффективную коррекцию порока одномоментно с реконструкцией ЛЖ и реваскуляризацией миокарда [3-5].
Анализируя результаты проведенного исследования выявлено, что операция геометрическая реконструкция ЛЖ и реваскуляризация миокарда в сочетании с коррекцией митральной регургитации улучшает качество жизни, приводит к восстановлению нормальной геометрии ЛЖ и уменьшает степень митральной недостаточности.
